第1章 基本概念
本章基本要求:
深刻理解熱力系統、外界、熱力平衡狀態、準靜態過程、可逆過程、熱力循環的概念,掌握溫度、壓力、比容的物理意義,掌握狀態參數的特點。
本章重點:resheji.com 整理
取熱力系統,對工質狀態的描述,狀態與狀態參數的關系,狀態參數,平衡狀態,狀態方程,可逆過程。
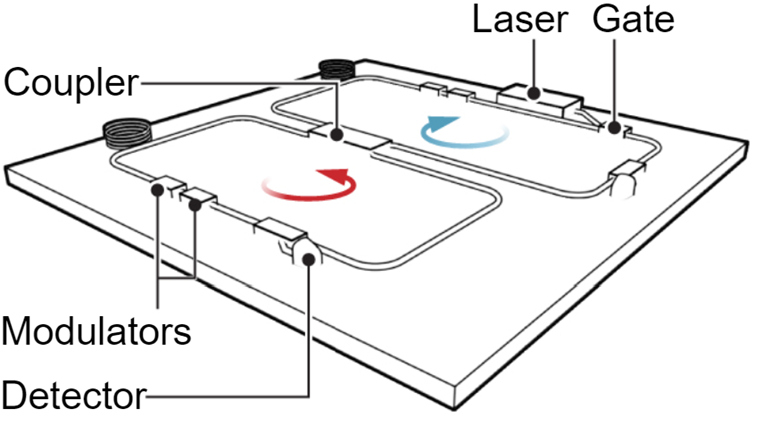
1. 1 熱力系統
一、熱力系統
系統:用界面從周圍的環境中分割出來的研究對象,或空間內物體的總和。
外界:與系統相互作用的環境。
界面:假想的、實際的、固定的、運動的、變形的。
二、閉口系統和開口系統(按系統與外界有無物質交換)
閉口系統:系統內外無物質交換,稱控制質量。
開口系統:系統內外有物質交換,稱控制體積。
三、絕熱系統與孤立系統
絕熱系統:系統內外無熱量交換 (系統傳遞的熱量可忽略不計時,可認為絕熱)
孤立系統:系統與外界既無能量傳遞也無物質交換
四、根據系統內部狀況劃分
可壓縮系統:由可壓縮流體組成的系統。
簡單可壓縮系統:與外界只有熱量及準靜態容積變化
均勻系統:內部各部分化學成分和物理'性質都均勻一致的系統,是由單相組成的。
非均勻系統:由兩個或兩個以上的相所組成的系統。
單元系統:一種均勻的和化學成分不變的物質組成的系統。
多元系統:由兩種或兩種以上物質組成的系統。
單相系:系統中工質的物理、化學性質都均勻一致的系統稱為單相系。
復相系:由兩個相以上組成的系統稱為復相系,如固、液、氣組成的三相系統。
注意:
系統的選取方法僅影響解決問題的繁復程度,與研究問題的結果無關。
思考題:
孤立系統一定是閉口系統嗎。反之怎樣。
孤立系統一定不是開口的嗎。
孤立系統是否一定絕熱。
1.2 工質的熱力狀態與狀態參數
一、狀態與狀態參數
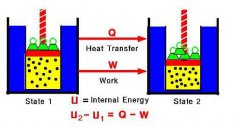
狀態:熱力系統中某瞬間表現的工質熱力性質的總狀況。
狀態參數:描述工質狀態特性的各種狀態的宏觀物理量。
如:溫度(T)、壓力(P)、比容(υ)或密度(ρ)、內能(u)、焓(h)、熵(s)、自由能(f)、自由焓(g)等。
1.3平衡狀態、狀態公理及狀態方程
標簽: 點擊: 評論: